Под качество природной воды в целом понимается характеристика ее состава и свойств, определяющая ее пригодность для конкретных видов водопользования (ГОСТ 17.1.1.01-77), при этом критерии качества представляют собой признаки, по которым производиться оценка качества воды.
Органолептические показатели
Любое знакомство со свойствами воды начинается с определения органолептических показателей, т.е. таких, для определения которых мы пользуемся нашими органами чувств (зрением, обонянием, вкусом).
Органолептическая оценка приносит много прямой и косвенной информации о составе воды. К таким характеристикам относятся: цветность, мутность (прозрачность), запах, вкус, привкус.
Мутность и прозрачность
Мутность воды вызвана присутствием тонкодисперсных примесей, обусловленных нерастворимыми или коллоидными неорганическими и органическими веществами различного происхождения.
Качественное определение проводят описательно: мутность не заметна (отсутсвует), слабая опалесценция (Прим.1) , опалесценция, слабомутная, мутная или сильно мутная. В России мутность чаще всего измеряют в нефелометрических единицах мутности НЕФ (NTU) для небольших значений в пределах 0-40 НЕФ (NTU), например для питьевой воды. В условиях большой мутности обычно применяется измерение единиц мутности по формазину (ЕФМ). Пределы измерений - 40-400 ЕФМ.
Когда вода имеет незначительные окраску и мутность, и их определение затруднительно, пользуются показателем "прозрачность".
Мера прозрачности - высота столба воды, при которой можно наблюдать опускаемую в воду белую пластину определенных размеров (диск Секки) или различать на белой бумаге шрифт определенного размера и типа (шрифт Снеллена). Результаты выражаются в сантиметрах (табл.1)
Таблица 1. Характеристика вод по прозрачности
|
Прозрачность |
Единица измерения, см |
|
Прозрачная |
Более 30 |
|
Маломутная |
От 25 до 30 |
|
Средней мутности |
От 20 до 25 |
|
Мутная |
От 10 до 20 |
|
Очень мутная |
Менее 10 |
Мутность не только отрицательно влиет на внешний вид воды. Главным отрицательным следствием высокой мутноти является то, что она защищает микроорганизмы при ультрафиолетовом обеззараживании и стимулирует рост бактерий. Поэому во всех случаях, когда производится дезинфекция воды, мутность должна быть минимальной для обеспечения высокой эффективности этой процедуры. В соответсвии с гигиеническими требованиями к качеству питьевой воды мутность не должна превышать 1,5 мг/л по каолину.
Запах
По характеру запахи делятся на две группы:
- естественного происхождения (живущие и отмершие в воде организмы, загнивающие растительные остатки и др.);
- искусственного происхождения (примеси промышленных и сельскохозяйственных сточных вод).
Интенсивность запаха оценивают по шестибальной шкале (табл.2)
Таблица 2. Характеристика вод по интенсивности запаха
|
Интенсивность запаха, баллы |
Характеристика |
Описательные определения |
|
0 |
Запаха нет |
Отсутствие ощутимого запаха |
|
1 |
Очень слабый |
Запах, не замечаемый потребителем, но обнаруживаемый опытным исследователем |
|
2 |
Слабый |
Запах, не привлекающий внимания потребителя, но обнаруживаемый им, если указать на него |
|
3 |
Заметный |
Запах, легко обнаруживаемый и могущий дать повод относиться к воде с неодобрением |
|
4 |
Отчетливый |
Запах, обращающий на себя внимание и делающий воду неприятной для питья |
|
5 |
Очень сильный |
Запах, сильный настолько, что делает воду непригодной для питья |
Таблица 3. Запахи естественного происхождения
|
Обозначение запаха |
Характер запаха |
Примерный род запаха |
|
А |
Ароматический |
Огуречный, цветочный |
|
Б |
Болотный |
Илистый, тинистый |
|
Г |
Гнилостный |
Фекальный, сточный |
|
Д |
Древесный |
Запах морской щепы, древесной коры |
|
З |
Землистый |
Прелый, запах свежевспаханной земли, глинистый |
|
П |
Плесневый |
Затхлый, застойный |
|
Р |
Рыбный |
Запах рыбьего жира, рыбы |
|
С |
Сероводородный |
Запах тухлых яиц |
|
Т |
Травянистый |
Запах скошенной травы, сена |
|
Н |
Неопределенный |
Запахи естественного происхождения, не подходящие под предыдущие определения |
Запахи второй группы (искуственного происхождения) называют по определяющим запах веществам: хлорный, бензиновый и т.д.
Вкус и привкус
Интенсивность вкуса и привкуса определяется также по 6-балльной шкале (табл.4)
Таблица 4. Характеристика вод по интенсивности вкуса
|
Оценка вкуса и привкуса, баллы |
Интенсивность вкуса и привкуса |
Характер проявления вкуса и привкуса |
|
0 |
Нет |
Вкус и привкус не ощущается |
|
1 |
Очень слабая |
Вкус и привкус сразу ощущается потребителем, но обнаруживаются при тщательном тестировании |
|
2 |
Слабая |
Вкус и привкус замечаются, если обратить на это внимание |
|
3 |
Заметная |
Вкус и привкус легко замечаются и вызывают неодобрительный отзыв о воду |
|
4 |
Отчетливая |
Вкус и привкус обращают на себя внимание и заставляют воздержаться от питья |
|
5 |
Очень сильная |
Вкус и привкус настолько сильны, что делают воду непригодной к употреблению |
Для питьевой воды допускаються значения показателй вкуса и привкуса не более 2 баллов.
Различают 4 вид вкусов:
- соленый
- горький
- сладкий
- кислый
Качественную характеристику оттенков вкусовых ощущений - привкуса - выражают описательно: хлорный, рыбный, горьковатый и так далее. Наиболее распространенный соленый вкус воды чащу всего обусловлен растворенным в воде хлоридом натрия, горький - сульфатом магния, кислый - избытком свободного диоксида углерода и т.д.
Цветность
Показатель качества воды, характеризующий интенсивность окраски воды и обусловленный содержанием окрашенных соединений, выражается в градусах платино-кобальтовой шкалы и определяется путем сравнения окраски испытуемой воды с эталонами.
Цветность природных вод обусловлена главным образом присутсвием гумусовых веществ и соединений трехвалентного железа, колеблется от единиц до тысяч градусов (табл.5)
Таблица 5. Характеристика вод по цветности
|
Цветность |
Единицы измерения, градус платино-кобальтовой шкалы |
|
Очень малая |
До 25 |
|
Малая |
Более 25 до 50 |
|
Средняя |
Более 50 до 80 |
|
Высокая |
Более 80 до 120 |
|
Очень высокая |
Более 120 |
Взвешенные примеси
Взвешенные твердые примеси, присуствующие в природных водах, состоят из частиц глины, песка, ила, суспедированных органических и неорганических веществ, планктона и различных микроорганизмов. Взвешенные частицы влияют на прозрачность воды.
Содержание в воде взвешенных примесей, измеряемое в мг/л, дает представление о загрязненности воды частицами, в основном, условным диаметром более 10 (в -4 степени) мм.
Водородный показатель (рН) 
Величина рН воды - один из важнейших показателей качества вод для определения тсабильности воды, ее накипеобразующих и коррозионных свойств, прогнозирования химических и биологических процессов, происходящих в природных водах. В зависимости от рН воду рационально делить на семь групп (табл.6)
Таблица 6. Классификация вод по рН
|
Группа воды |
рН |
|
Сильнокислая |
Менее 3,0 |
|
Кислая |
Более 3,0 до 5,0 |
|
Слабокислая |
Более 5,0 до 6,5 |
|
Нейтральная |
Более 6,5 до 7,5 |
|
Слабощелочная |
Более 7,5 до 8,5 |
|
Щелочная |
Более 8,5 до 9,5 |
|
Сильнощелочная |
Более 9,5 |
От величины рН зависит развитие и жизнедеятельность многих организмов, агрессивное действие воды на металлы и бетон. Величина рН воды также влияет на процессы превращения различных форм биогенных элементов, изменяет токсичность загрязняющих веществ.
В соответсвии с требованиями к составу и свойствам питьевой воды, величина рН не должна выходить за пределы интервала значений 6,0-9,0. Контроль уровня рН особенно важен на всех стадиях водоочистки, так как его "уход" в ту или иную сторону может не только существенно сказаться на запахе, привкусе и внешнем виде воды, но и повлиять на эффективность водоочистных мероприятий.
При низком рН вода обладает высокой коррозионной активностью, а при высоких уровнях (рН>11) вода приобретает характерную мылкость, неприятный запах, вызывает раздражение глаз и кожи.
Минерализация
Минерализация - суммарное содержание всех найденных при химическом анализе воды минеральных веществ. Минерализация природных вод, определяющая их удельную электропроводность, изменяется в широких пределах. Большинство рек имеет минерализацию от нескольких десятков миллиграммов в литре до нескольких сотен. Их удельная электропроводимость варьируется от 30 до 1500 мкСм/см. Минерализация подземных вод и соленых озер изменяется в интервале от 40-50 мг/л до сотен г/кг (плотность в этом случае уже значительно отличается от единицы). Удельная электропроводимость атмосферных осадков с минерализацией от 3 до 60 мг/л составляет значения 10-120 мкСм/см.
Таблица 7. Характеритика вод по минерализации 
|
Группа воды |
Единица измерения, г/л |
|
Пресные |
До 1 |
|
Солоноватые |
Более 1 до 25 |
|
Соленые |
Более 25 до 50 |
|
Рассолы |
Более 50 |
Предел пресных вод - 1 г/л - установлен в связи с тем, что при минерализации более этого значения вкус воды неприятен - соленый или горько-соленый.
Предел - граница между солоноватыми и солеными водами - принят на том основании, что при минерализации около 25 г/л температура замерзания воды и температура наибольшей плотности морской воды совпадают, и при этом меняются некоторые свойства воды.
Граница 50 г/л между солеными водами и рассолами обусловлена тем, что соленость больше этого значения не бывает в морях; Такая соленость характерна только для соленых озер и некоторых подземных вод.
Таблица 8. Характеристика вод по общей минерализации (наиболее распространеннная градация) 
|
Наименование воды |
Общая минерализация, г/л |
|
Ультрапресная |
До 0,1 |
|
Пресная |
Более 0,1 до 1,0 |
|
Слабопресная |
Более 1,0 до 3,0 |
|
Соленая |
Более 3,0 до 10,0 |
|
Сильносоленая |
Более 10,0 до 50,0 |
|
Рассол |
Более 50,0 до 300,0 |
|
Ультрарассол |
Более 300,0 |
В соответствии с гигиеническими требованиями к качеству питьевой воды суммарная минерализация не должна превышать 1000 мг/л. Вода содержащая большое количество солей, отрицательно влияет на растения и человека, вызывает образование накипи на стенках котлов, коррозию, засоление почв. Регулярное употребление высокоминерализированной воды приведет к болезням пищеварения, обмена веществ, повышеной сухости кожи.
Жесткость
Жесткость воды обуславливается наличием в воде ионов кальция, магния, стронция, бария, железа, марганца. Но общее содержание в природных водах ионов кальция и магния несравнимо больше содержания всех других перечисленных ионов - и даже их суммы. Поэтому под жесткостью понимают сумму количеств ионов кальция и магния - общая жесткость, складывающаяся из значений карбонатной (временной, устраняемой кипячением) и некарбонатной (постоянной) жесткости. Первая вызвана присутствием в воде гидрокарбонатов кальция и магния, вторая - наличием сульфатов, хлоридов, силикатов, нитратов и фосфатов этих металлов. Однако при значении жесткости воды более 9 ммоль/л нужно учитывать содержание в воде стронция и других щелочноземельных металлов.
По стандарту ИСО 6107-1-8: 1996, включающему более 500 терминов, жесткость определяется как способность воды образовать пену мылом. Содержание в питьевой воде кальция и магния играет важнейшую роль для человеческого организма. Недостаточность кальция в организме негативно сказывается на функии сердечной мышцы и на активности некоторых ферментов. А недостаток содержания кальция в крови ведет к понижению возбуждаемости нервной системы и, как следствие, к возникновению судорог. Кальций необходим для формирования костных тканей, в том числе зубов. Соли магния тоже необходимы человеку, поскульку входят в ряд жизненно важных ферментов. Дефицит магния проводит к коронарной болезни сердца; с другой стороны, повышенное содержание магния угнетающе действуют на нервную систему, поражая двигательные нервные окончания.
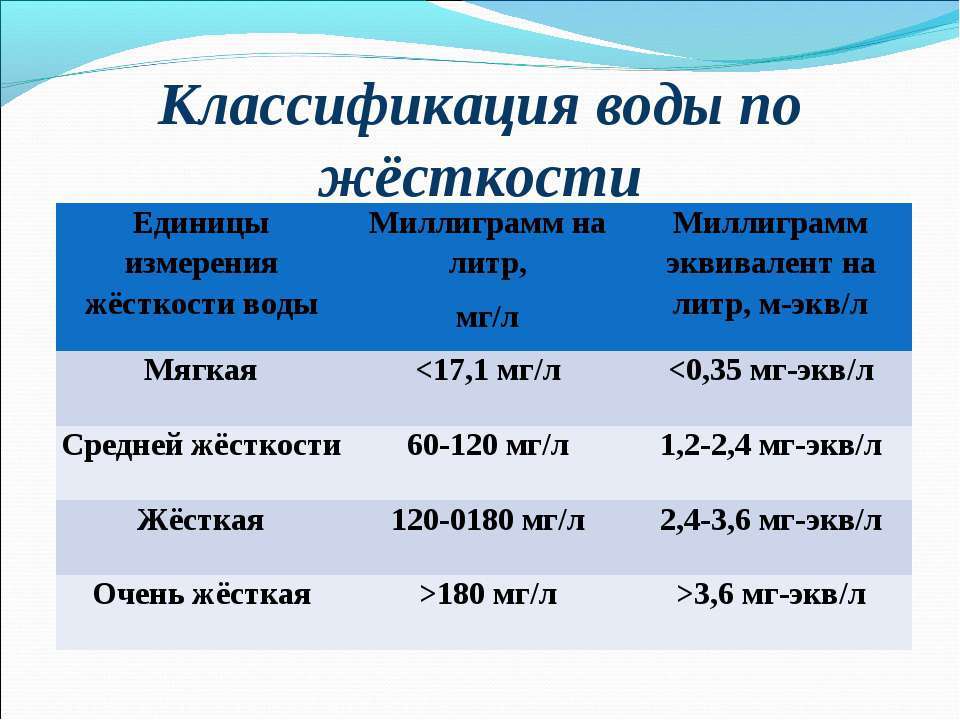
По значению общей жесткости природные воды делят на группы (табл.9)
Таблица 9. Классификация воды по жесткости
|
Группа воды |
Единица измерения, ммоль/л |
|
Очень мягкая |
До 1,5 |
|
Мягкая |
Более 1,5 до 4,0 |
|
Средней жесткости |
Более 4 до 8 |
|
Жесткая |
Более 8 до 12 |
|
Очень жесткая |
Более 12 |
В естественных условиях ионы кальция и магния определяющие жесткость, поступают в воду в результате взаимодействия растворенного диоксида углерода с карбонатными минералами и других процессов растворенияи химического выветривания горных пород. Источником этих ионов являются также микробиологические процессы, протекающие в почвах. Обычно преобладает жесткость, обусловленая ионами кальция (до 70%); однако в отдельных случаях магниевая жесткость может достигать 50-60%. Жесткость морской воды и океанов значительно выше (десятки ммоль/л). Жесткость поверхностных вод подвержена заметным сезонным колебаниям, достигая обычно наибольшего значения в конце зимы и наименьшего - в период половодья.
Росстандартом в качестве единицы жесткости воды установлен моль на кубический метр (моль/м3). Один моль на кубический метр соответствует массовой концентрации эквивалентов ионов кальция 20,04 г/м3 (мг/л) или ионов магния 12,153 г/м3 (мг/л). Т.е., 1 моль/м3 = 1 ммоль/л = 1 мг-экв/л - 1 мг-экв/дм3 . В зарубежных странах широко используются такие единицы жесткости, как немецкий градус (do, dH), французский градус (fo), американский градус (ppm CaCO³).
Основные единицы жесткости воды и их соотношение:
|
Моль/м3 (мг-экв/л)
|
Немецкий градус, do |
Французский градус,fo |
Английский градус |
Американский градус |
gpg (grain per gallon, или грэйн/галлон) |
Ppm (мг/л) CaCO3 |
|
1.000 |
2.804 |
5.005 |
3.511 |
50.050 |
2.920 |
50.050 |
Прим.1 Опалесценция - "[опал + лат. -escenua суффикс, означающий слабое действие] — физ. явление рассеяния света мутной средой, обусловленное ее оптической неоднородностью; наблюдается, напр. , при освещении большинства коллоидных растворов, а также у веществ в критическом состоянии
Опалесценция критическая - резкое усиление рассеяния света чистыми веществами (газами или жидкостями) в критических состояниях, а также растворами при достижении ими критических точек смешения.
Повышенная жесткость воды негативно отражается на здоровье человека. В быту появление накипи приводит к уменьшению срока слыжбы водонагревателей, ухудшаются моющие свойства мыла и стиральных порошков, из-за горьковатого привкуса ухудшаются вкусовые свойства воды.
Порог вкуса для иона кальция лежит в диапазоне 2-6 ммоль/л, в зависимости от соответствующего аниона. Порог вкуса для магния и того ниже, наилучшие вкусовые свойства имеет вода с жсткостью 1,6-3,0 ммоль/л.
Всемирная организация здравоохранения (ВОЗ) не регламентирует величину жесткости по показаниям влияния на здоровье. В материалах ВОЗ говориться о том, что несмотря на выявленную статистическим путем зависимость между жесткостью питьевой воды и сердечно-сосудистыми заболеваниями, этих данных недостаточно для вывода о причинном характере этой связи. Однозначно не доказано и то, что мягкая вода оказывает отрицательный эффект на баланс минеральных веществ в организме человека.
Растворенный кислород 
Поступление кислорода в водоем происходит путем растворения его при контакте с воздухом (абсорбции), а также в результате фотосинтеза водными растениями, т.е. в результате физико-химических и биохимических процессов. Содержание растворенного кислорода зависит от температуры, атмосферного давления, степени турбулизации воды*, минерализации воды и др. В поверхностных водах содержание растворенного кислорода может колебаться от 0 до 14 мг/л и подвержено значительным сезонным суточным колебаниям. В зимний и летний периоды количество кислорода в воде различается. Дефицит кислорода чаще наблюдается в водных объектах с высокими концентрациями загрязняющих органических веществ и в водоемах, содержащих большое количество биогенных и гумусовых веществ. ПДК растворенного в воде кислорода для рыбохозяйственных водоемов - 6 мг/л (для ценных пород рыбы) и 4 мг/л (для остальных пород рыбы).
Скорость потребления кислорода увеличивается с повышением температуры, количества организмов и веществ, подвергающихся химическому и биохимическому окислению.
Концентрация кислорода в воде определяет направление и скорость процессов химического и биохимического окисления органических и неорганических соединений. Понижение содержания кислорода до 2 мг/л вызывает массовую гибель рыбы в водоемах. Неблагоприятно сказывается на состоянии водных объектов и чрезмерное насыщение воды кислородом в результате процессов фотосинтеза, если это происходит в водоемах с застойной водой.
Содержание кислорода в водоемах с различной степенью загрязненности:
Таблица 10. Уровень загрязнения воды и класс качества
| Растворенный кислород | |||
| Очень чистые, I | лето, мг/л | зима, мг/л | % насыщения |
| Чистые, II | 9 | 14-13 | 95 |
| Умеренно загрязненные, III | 8 | 12-11 | 80 |
| Загрязненные, IV | 7-6 | 10-9 | 70 |
| Грязные, V | 5-4 | 5-4 | 60 |
| Очень грязные, VI | 3-2 | 5-1 | 30 |
| 0 | 0 | 0 | |
*Турбулизация приводит к нарушению поверхностного натяжения воды. При этом разрывается поверхностная пленка и облегчается выход газов из воды. Благодаря турбулентному движению происходит перемешивание частиц воды и непрерывное обновление поверхности соприкосновения воды с паром. Это ускоряет выход газа из воды и переход его в пар. Турбулизация движения воды создается потоком пара, пересекающим струи воды.

 Нитраты являются солями азотной кислоты. Повышенное содержание нитратов в воде может служить индикатором загрязнения водоема в результате распространения фекальных либо химических загрязнений (сельскохозяйственных, промышленных). Согласно СанПин 2.1.4.1074-01 для питьевой воды ПДК нитратов составляет 45 мг/л. Питьвая вода и продукты питания, содержание повышенное количество нитратов, могут вызывать заболевания, в первую очередь у младенцев (так называемая метгемоглобинемия), а также людей, страдающих сердечно-сосудистыми заболеваниями. Допустимое суточное потребление по рекомендациям ВОЗ - 5 мг/кг массы. В этом случае особенно опасны грунтовые воды и питаемые ими колодцы, поскольку в открытых водоемах нитраты частично потребляются водными растениями. Вместе с тем, растения не так чувствительны к увеличению содержания в воде азота, как фосфора.
Нитраты являются солями азотной кислоты. Повышенное содержание нитратов в воде может служить индикатором загрязнения водоема в результате распространения фекальных либо химических загрязнений (сельскохозяйственных, промышленных). Согласно СанПин 2.1.4.1074-01 для питьевой воды ПДК нитратов составляет 45 мг/л. Питьвая вода и продукты питания, содержание повышенное количество нитратов, могут вызывать заболевания, в первую очередь у младенцев (так называемая метгемоглобинемия), а также людей, страдающих сердечно-сосудистыми заболеваниями. Допустимое суточное потребление по рекомендациям ВОЗ - 5 мг/кг массы. В этом случае особенно опасны грунтовые воды и питаемые ими колодцы, поскольку в открытых водоемах нитраты частично потребляются водными растениями. Вместе с тем, растения не так чувствительны к увеличению содержания в воде азота, как фосфора. 




 Спектр органических примесей очень широк:
Спектр органических примесей очень широк: Гидрохимический индекс загрязнения воды
Гидрохимический индекс загрязнения воды